Estados Físicos da Água
A água é encontrada na natureza em três estados físicos, a saber: Líquido, Sólido e Gasoso.
Assim, o ciclo da água corresponde ao movimento da água da natureza e, portanto, apresenta os processos de transformação da água.
Em outras palavras, as mudanças dos estados físicos da água ocorrem por meio dos processos denominados: Fusão, Vaporização (Ebulição e Evaporação), Solidificação, Liquefação (Condensação) e Sublimação.
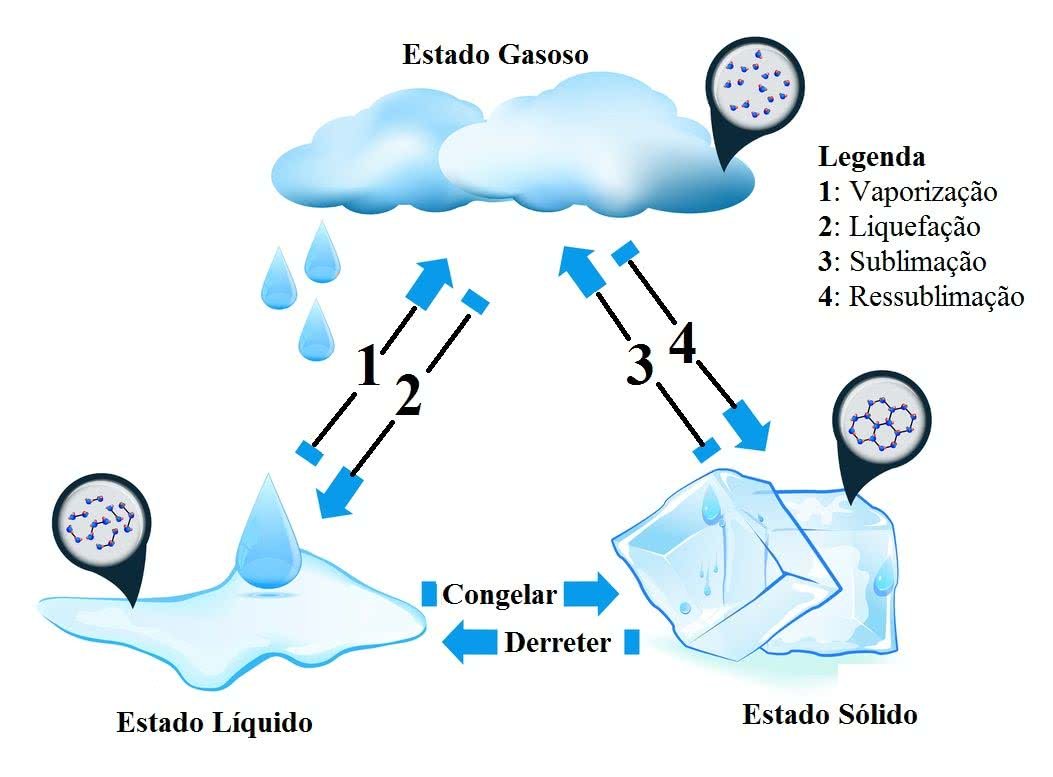 Mudanças de Estado Físico
Mudanças de Estado Físico
Para saber mais: Água e Ciclo da Água
Os Três Estados Físicos da Água
Dependendo de sua forma, a água pode ser encontrada de três maneiras:
Estado Líquido
Encontrada em maior parte no planeta por meio de rios, lagos e oceanos; o estado líquido não possui forma própria.
Estado Sólido
No estado sólido, a água possui forma, como por exemplo, os cubos de gelos. Isso acontece pois as moléculas de água encontram-se muito próximas devido à temperatura.
Estado Gasoso
No estado gasoso, as partículas de água encontram-se afastadas umas das outras e, por isso, não possui uma forma definida.
Mudanças de Estados Físicos da Água
As Mudanças de Estados Físicos da Água são divididas em 5 processos, a saber:
Fusão
Mudança do estado sólido para o estado líquido da água, provocada por aquecimento, por exemplo, um gelo que derrete num dia de calor.
Além disso, o denominado "Ponto de Fusão" (PF) é a temperatura que a água passa do estado sólido para o líquido. No caso da água, o ponto de fusão é de 0ºC.
Vaporização
Mudança do estado líquido para o estado gasoso por meio do aquecimento da água. Assim, o "Ponto de Ebulição" (PE) de uma substância é a temperatura a que essa substância passa do estado líquido para o estado gasoso e, no caso da água, o é de 100ºC.
Vale lembrar que a Ebulição e a Evaporação são, na realidade, tipos de vaporização. A diferença de ambas reside na velocidade do aquecimento, ou seja, se for realizado lentamente chama-se evaporação; entretanto, se for realizado com aquecimento rápido chama-se ebulição.
Solidificação
Mudança de estado líquido para o estado sólido provocado pelo arrefecimento ou resfriamento. Além disso, o "Ponto de Solidificação" da água é de 0ºC. O exemplo mais visível são os cubos de água que colocamos no refrigerador para fazer os cubos de gelo.
Liquefação
Chamada também de Condensação, esse processo identifica a mudança do estado gasoso para o estado líquido decorrente do resfriamento (arrefecimento). Como exemplo podemos citar: a geada e o orvalho das plantas.
Sublimação
Mudança do estado sólido para o estado gasoso, por meio do aquecimento. Também denomina a mudança do estado gasoso para o estado sólido (ressublimação), por arrefecimento, por exemplo: gelo seco e naftalina.
Leia também sobre: